Einleitung
Equipmentfehler zählen zu den häufigsten Ursachen für Abweichungen, Qualitätsprobleme und ungeplante Stillstände in analytischen und diagnostischen Laboren. Ob im GMP-Labor, GLP-Labor oder in nach DIN EN ISO/IEC 17025 bzw. ISO 15189 akkreditierten Einrichtungen – der strukturierte Umgang mit Gerätefehlern ist entscheidend für valide Ergebnisse und durchgängige Datenintegrität.
Dennoch setzen zahlreiche Laboratorien weiterhin auf Excel-Listen, dezentrale Dokumentation oder Papierlogbücher für die Prüfmittelverwaltung, Messmittelüberwachung und Messmittelverwaltung. Diese Vorgehensweise bringt erhebliche Risiken mit sich: fehlende Versionierung, keine Audit-Trails, uneinheitliche Nomenklatur, Medienbrüche und erschwerte Trendanalysen.
Mit steigender regulatorischer Komplexität gewinnen Labor-Digitalisierung, professionelles Lab Equipment Management, Labormanagement Software und prozessorientierte Prüfmittelverwaltungssoftware zunehmend an Bedeutung – nicht nur zur Effizienzsteigerung, sondern vor allem zur Absicherung der Compliance.

Was sind Equipmentfehler?
Equipmentfehler entstehen an Messgeräten, Prüfmitteln, Laborinstrumenten oder automatisierten Systemen und lassen sich in mehrere Kategorien einteilen.
Technische Fehlermeldungen
Hierzu gehören Pumpenausfälle, Ventilfehler und Druckinstabilitäten sowie Temperaturdrift in Inkubatoren oder Öfen. Auch Sensorfehler wie UV-Lampenalterung oder Detektordrift fallen in diese Kategorie. Diese technischen Störungen erfordern häufig eine unmittelbare Reaktion und können den Messbetrieb komplett unterbrechen.
Abweichende Messwerte & Drift
Unerwartete Standardabweichungen, unplausible Peaks oder Signale sowie instabile Grundlinien deuten auf systematische Probleme hin. Diese Fehler betreffen direkt die Prüfmittelüberwachung und Kalibrierung und können eine erneute Qualifizierung erforderlich machen.
Kalibrierfehler
Überfällige Kalibrierfristen, fehlende Nachweise oder falsch angewendete Kalibrierprozeduren stellen ein erhebliches Compliance-Risiko dar. Die Anforderungen an die Prüfmittelüberwachung Kalibrierung sind in DIN EN ISO IEC 17025 (auch bekannt als DIN ISO EN 17025, DIN EN ISO 17025 oder DIN ISO IEC 17025) detailliert beschrieben und müssen konsequent umgesetzt werden.
Dokumentationsfehler (ALCOA-Prinzip)
Typische Probleme bei papierbasierter oder Excel-gestützter Dokumentation (Prüfmittelüberwachung Excel) sind fehlende Zeitstempel, unklare Zuordnungen, nachträgliche Änderungen ohne Audit Trail sowie fehlende Personenzuordnung. Diese Mängel widersprechen dem ALCOA Prinzip und gefährden die Datenintegrität.
Bedienungsfehler
Unklare SOPs, falsche Parametrisierung oder fehlendes Training führen häufig zu wiederkehrenden Fehlern. Diese Kategorie zeigt deutlich die Bedeutung von systematischem Labormanagement, strukturiertem Wissensmanagement und insbesondere professionellem Labor Wissensmanagement zur Vermeidung von Bedienfehlern.
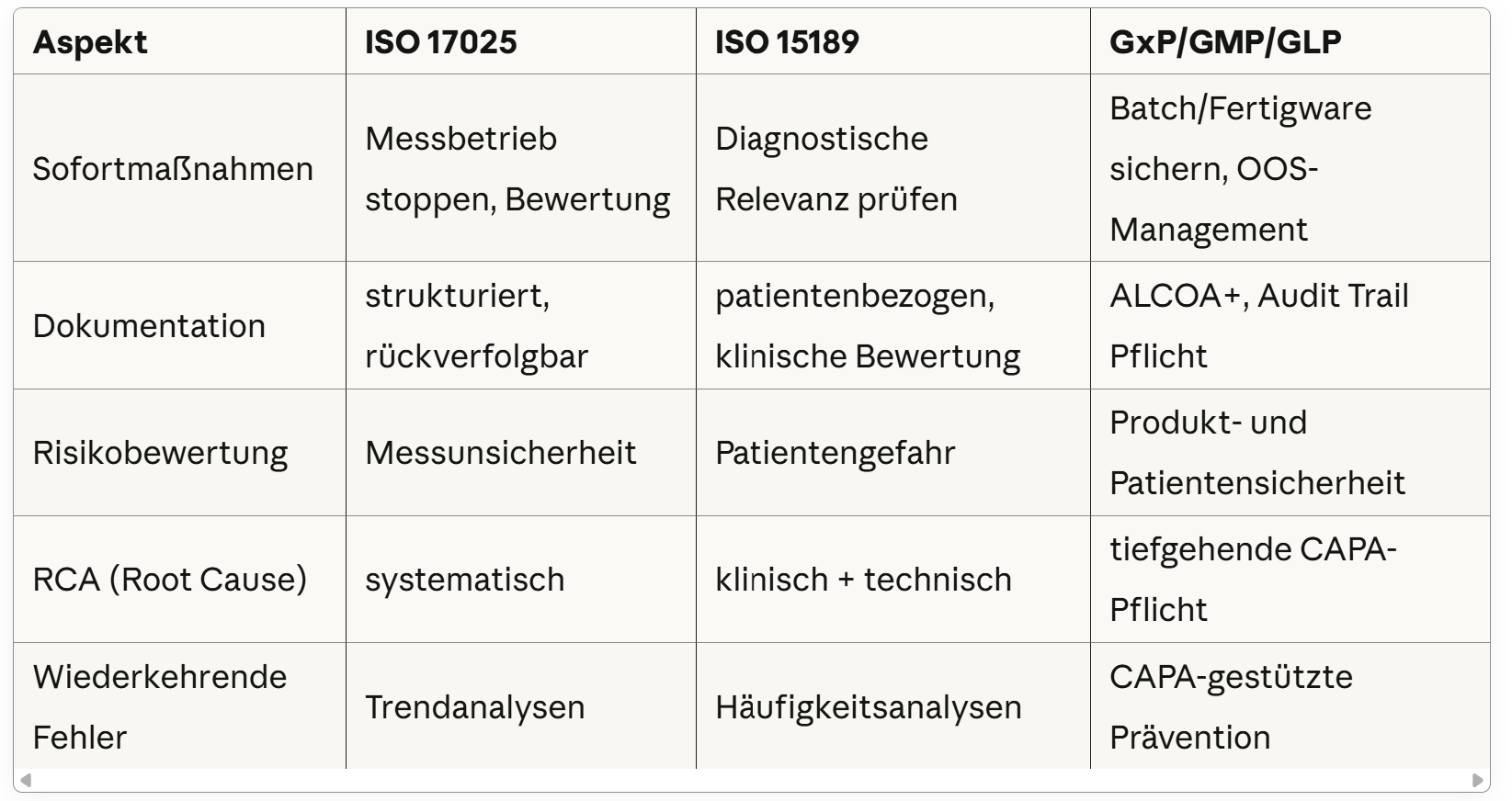
Tabellarischer Vergleich der Unterschiede im Fehlermanagement zwischen ISO 17025, ISO 15189 und GxP/GMP/GLP – jeweils mit Fokus auf Sofortmaßnahmen, Dokumentation, Risikobewertung, Root Cause Analysis und wiederkehrende Fehler.
Die drei Normsysteme im Überblick
DIN EN ISO/IEC 17025
Der Fokus liegt auf Messmittelüberwachung, Prüfmittelmanagement inklusive Rückverfolgbarkeit, regelmäßiger Kalibrierung und Verifizierung sowie der Dokumentation von Abweichungen. Zusätzlich ist die Bewertung der Messunsicherheit erforderlich. Der Umgang mit Equipmentfehlern muss nachvollziehbar, bewertbar und reproduzierbar dokumentiert werden. Die Norm wird häufig auch als DIN ISO 17025 oder DIN EN ISO 17025 bezeichnet.
DIN EN ISO 15189
Für medizinische Labore gelten besondere Anforderungen aufgrund der direkten Auswirkung auf die Patientensicherheit und die Validität diagnostischer Ergebnisse. Es bestehen strengere Anforderungen an Reaktionszeiten, Bewertung und CAPA sowie eine enge Verknüpfung von Gerätefehlern und klinischen Entscheidungen.
GxP/GMP/GLP
Die GxP-Regularien erwarten vollständige Datenintegrität nach ALCOA+, lückenlose Audit Trails, qualifizierte Lieferanten sowie dokumentierte Gerätequalifizierungen (IQ/OQ/PQ). Sowohl im GMP Labor als auch im GLP Labor ist eine strukturierte Prüfmittelverwaltung und die Dokumentation von GLP Equipment mit vollständigen Lebenszyklen erforderlich. Fehler müssen in digital manipulationssicheren Systemen nachvollziehbar dokumentiert werden.
Gemeinsame Grundlogik aller Normen
Trotz unterschiedlicher Schwerpunkte folgen alle drei Systeme einem einheitlichen Kernprozess:
- Fehler erkennen
- Gerät stoppen bzw. isolieren
- Bewertung (Risiko, Validität, Auswirkungen)
- Ursachenanalyse (RCA)
- Korrekturmaßnahmen
- Präventivmaßnahmen (CAPA)
- Wirksamkeitsprüfung
- Dokumentation im Audit Trail
Diese Schritte bilden die Grundlage für digitales Equipment Management, strukturiertes Prüfmittelmanagement, professionelle Prüfmittelverwaltung Software sowie modernes Laboratory Management.
Moderne Lösungsansätze
Labor-Digitalisierung
Digitale Systeme automatisieren die Dokumentation, verbinden Messwertdaten mit Logbüchern und Gerätestatus und unterstützen normkonforme Abläufe. Sie eliminieren Medienbrüche und schaffen durchgängige Transparenz.
Digitale Prüfmittelverwaltungssoftware
Professionelle Prüfmittelmanagement Software überwacht Kalibrierfristen automatisch, führt Historien lückenlos, weist proaktiv auf Risiken hin und ersetzt fehleranfällige Excel-Lösungen. Während kostenlose Prüfmittelüberwachung Software kostenlos erste Lücken schließen kann, stößt sie bei GxP-Audits schnell an ihre Grenzen hinsichtlich Audit Trail, Validierung und Datenintegrität.
Automatisierte Messmittelüberwachung
Moderne Systeme integrieren Echtzeitdaten, Wartungszyklen, Kalibrierintervalle, Nutzungsdaten und Driftanalysen in einer zentralen Plattform. Dies ermöglicht eine proaktive statt reaktive Instandhaltungsstrategie.
Predictive Maintenance
Durch die Analyse von Nutzungsdaten können Fehler und Abweichungen prognostiziert werden, bevor sie tatsächlich auftreten. Dies reduziert ungeplante Ausfallzeiten signifikant und verbessert die Planbarkeit.
Lab Equipment Management Systeme
Diese Systeme bilden das Zentrum modernen Labormanagements mit zentraler Asset-Verwaltung, manipulationssicheren Audit Trails, Echtzeit-Statusmonitoring und digitalen Logbüchern.
Wie LabThunder Equipmentfehler managt
LabThunder kombiniert Labor-Digitalisierung, Equipment Management, Prüfmittelverwaltungssoftware und KI-gestütztes Troubleshooting in einem normkonformen Ansatz für ISO 17025-, ISO 15189- und GxP-Labore.
Früherkennung von Gerätefehlern
Das System erfasst kontinuierlich Gerätestatus, Nutzungsdaten und Logbucheinträge. Durch automatische Erkennung auffälliger Trends (beispielsweise Detektordrift, Druckanstieg oder ungewöhnliche Peaks) können potenzielle Probleme frühzeitig identifiziert werden.
Digitale Logbücher
LabThunder bietet manipulationssichere Audit Trails nach ALCOA-Prinzip, strukturierte Erfassung von Fehlern, Abweichungen und Maßnahmen sowie eine direkte Verknüpfung mit Kalibrier- und Wartungshistorie.
Integrierte Prüfmittelverwaltung
Die automatische Kalibrierüberwachung mit Fristerinnerung, zentrale Dokumentation der Prüfmittel- und Messmittelhistorie sowie lückenlose Rückverfolgbarkeit erfüllen die Anforderungen von DIN EN ISO 17025, ISO 15189 und GLP Equipment Management.
Predictive Maintenance
Durch die Nutzung von Trends aus Logbüchern, Sensorwerten und Nutzungshäufigkeit werden ungeplante Stillstände minimiert und die Verfügbarkeit der Geräte optimiert.
Thunder AI für technisches Troubleshooting
Die KI-Komponente analysiert Fehlerbilder, Logbucheinträge und Wartungshistorien, schlägt wahrscheinliche Ursachen vor, verweist auf relevante Passagen aus Handbüchern und unterstützt die Root Cause Analysis.
Warum LabThunder Excel ersetzt
- Vollständiger Audit Trail statt manueller Versionierung
- Keine Medienbrüche zwischen verschiedenen Systemen
- Normative Abbildung aller regulatorischen Anforderungen
- Echtzeit-Equipmentstatus für alle Stakeholder
- Automatisierte Fehler- und Wartungserkennung
LabThunder ermöglicht ein strukturiertes Fehlermanagement, das sowohl kleinere Labore als auch komplexe GxP-Umgebungen normkonform unterstützt.
FAQ zum Fehlermanagement im Labor
Was sind typische Equipmentfehler in Laboren?
Pumpenfehler, Drift, Sensorinstabilität, Temperaturabweichungen, Kalibrierfehler, Softwarefehler, Bedienungsfehler, Dokumentationslücken und unvollständige Logbücher.
Was ist der Unterschied zwischen Messmittelüberwachung und Prüfmittelverwaltung?
Messmittelüberwachung fokussiert auf Kalibrierung und Verifizierung. Prüfmittelverwaltung umfasst zusätzlich Wartung, Qualifizierung, Historie, Dokumentation und Einsatzplanung.
Welche Rolle spielt das ALCOA-Prinzip bei Gerätefehlern?
Es definiert Anforderungen an Datenintegrität: Attributable, Legible, Contemporaneous, Original, Accurate. Fehlerdokumentation muss vollständig, nachvollziehbar und manipulationssicher erfolgen.
Warum reichen Excel-Listen für Prüfmittelüberwachung nicht mehr aus?
Excel bietet keine Audit Trails, keine Benutzerverwaltung, keine Automatisierung, keine Verknüpfung zu Logbüchern oder Wartungszyklen und ist anfällig für Fehler. Für ISO 17025, ISO 15189 und GMP ist es nicht ausreichend.
Wie hilft LabThunder konkret beim Fehlermanagement?
Durch digitale Logbücher, KI-gestützte Fehleranalyse, automatisierte Prüfmittelüberwachung, Predictive Maintenance, normkonforme Dokumentation und Echtzeit-Equipmentstatus.


LabThunder:
✅ Compliant nach ISO 17025, GMP/GLP und ISO 15189
✅ Digitale Logbücher statt Zettelchaos
✅ Thunder AI - zentrale Intelligenz bei Fehlern & Fragen
✅ Smarte & Predictive Maintenance verhindert Ausfälle
✅ Mehr Unabhängigkeit von externem Service
✅ bis zu 50 % weniger Serviceeinsätze
✅ easy to use - keine IT nötig
Kontaktieren Sie uns noch heute für einen kostenfreie Demo:






%20new.png)















.jpg)
.jpg)

